- Вольфрамовая кислота
-
Вольфрамовая кислота 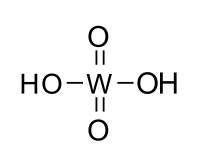
Общие Традиционные названия ортовольфрамовая кислота Химическая формула H2WO4 Эмпирическая формула H2O4W Физические свойства Состояние (ст. усл.) желтое кристаллическое или аморфное вещество Молярная масса 249.85 г/моль Плотность 5.59 г/см³ Термические свойства Температура плавления 100 °C Температура кипения 1473 °C Молярная теплоёмкость (ст. усл.) 119,9 Дж/(моль·К) Энтальпия образования (ст. усл.) -1132 кДж/моль Химические свойства Растворимость в воде плохая Растворимость в кислотах плохая, за исключением HF и аммония Классификация Рег. номер CAS 7783-03-1 SMILES O.O=[W](=O)=O RTECS YO7840000 Безопасность Токсичность Вольфрамовая кислота — моногидрат триоксида вольфрама — WO3·H2O, вопреки часто распространенному мнению формула H2WO4 не отвечает действительной структуре соединения. Впервые кислота была получена Карлом Вильгельмом Шееле в 1781 году.
Содержание
Свойства
Адсорбент, катализатор гидрогенизации. Реагирует с щелочами, фтороводородом, раствором аммиака.
При нагревании выше 100°C разлагается на Оксид вольфрама(VI) и воду:
Получение
Получается при действии сильных кислот на растворы вольфраматов щелочных металлов. Вольфрам в смеси азотной и плавиковой кислот растворяется, образуя вольфрамовую кислоту. Триоксид вольфрама не растворяется в воде. Получить вольфрамовую кислоту можно следующим образом:
Так же она получается при действии карбоната водорода и вольфрамата натрия:
Применение
Применяется как протрава и краситель в текстильной промышленности. Вольфрамовая кислота является промежуточным продуктом в производстве вольфрама, используется в качестве протравы при крашении тканей.
Остальное
Кислота довольно дорогая; цена за 1 грамм достигает примерно 200 рублей. На вольфрамовую кислоту распространяется ГОСТ под номером 2197-78[1]
Примечания
- ↑ Библиотека ГОСТов (рус.) (последняя редакция от 01.12.1989). Архивировано из первоисточника 18 июня 2012. Проверено 22 марта 2010.
Категории:- Соединения вольфрама
- Неорганические кислородсодержащие кислоты
- Моногидраты
- Соединения водорода
Wikimedia Foundation. 2010.




