- Медный купорос
-
Сульфат меди(II) 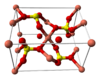
Общие Систематическое наименование Меди(II) сульфат Традиционные названия Медный купорос Химическая формула CuSO4 Молярная масса 159,61 г/моль Физические свойства Плотность вещества 3,60 г/см³ Термические свойства Температура плавления 110 °C Химические свойства pKa 5·10-3 Растворимость в воде 31.6 г/100 мл Структура Координационная геометрия Октаэдрическая Кристаллическая структура Триклинная Классификация номер CAS 7758-98-7 RTECS GL8800000 Сульфат меди(II) — (CuSO4) — бесцветные кристаллы, хорошо растворимые в воде. Однако из водных растворов, а также на воздухе хотя бы с незначительным содержанием влаги кристаллизуется голубой пентагидрат CuSO4 · 5H2O — медный купорос. Благодаря этому свойству сульфат меди(II) иногда используется в качестве индикатора влажности помещения.
 Сульфат меди CuSO4 · 5H2O
Сульфат меди CuSO4 · 5H2OСодержание
Строение кристаллогидрата
Структура медного купороса приведена на рисунке. Как видно, вокруг иона меди координированы два аниона SO42- по осям и четыре молекулы воды (в плоскости), а пятая молекула воды играет роль мостиков, которые при помощи водородных связей объединяют молекулы воды из плоскости и сульфатную группу.
Свойства
При нагревании последовательно отщепляет две молекулы воды, переходя в тригидрат CuSO4 · 3H2O (этот процесс, то есть выветривание частично идёт и просто на воздухе), затем в моногидрат (110°) CuSO4 · H2O, и выше 258 °C образуется безводная соль. Термическое разложение становится заметным выше 650°С:
CuSO4 →(t) CuO + SO2↑ + O2↑ Растворимость CuSO4, г/100 г H2O
Растворимость CuSO4, г/100 г H2OРастворимость сульфата меди(II) по мере роста температуры проходит через плоский максимум (см. рис.)
Как и все соли, образованные ионами слабого основания и сильной кислоты, сульфат меди(II) гидролизуется, (степень гидролиза в 0,01М растворе при 15 °C составляет 0,05 %) и даёт кислую среду (pH указанного раствора 4,2). Константа диссоциации составляет 5·10-3.
С сульфатами щелочных металлов и аммония образует комплексные соли, например, Na2[Cu(SO4)2]·6H2O.
Окрашивает огонь в зелёный цвет.
 Кристаллы сульфата меди (II), выращенные в домашних условиях
Кристаллы сульфата меди (II), выращенные в домашних условияхПрименение
Сульфат меди(II) наиболее важная соль меди, часто служит исходным сырьём для получения других соединений.
Безводный сульфат меди можно использовать как индикатор влажности, с его помощью в лаборатории проводят осушку этанола и некоторых других веществ.
Наибольшее количество непосредственно применяемого CuSO4 расходуется на борьбу с вредителями в сельском хозяйстве, в составе бордосской смеси с известковым молоком — от грибковых заболеваний и виноградной тли.
В строительстве водный раствор сульфата меди применяется для нейтрализации последствий протечек, ликвидации пятен ржавчины, а так же для удаления выделений солей («высолов») с кирпичных, бетонных и оштукатуренных поверхностей; а также как средство для предотвращения гниения древесины.
Также он применяется для изготовления минеральных красок, в медицине, как один из компонентов электролитических ванн для меднения и т. п. и как часть прядильных растворов в производстве ацетатного волокна.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E519 (консервант).
В природе изредка встречается минерал Халькантит, состав которого близок к CuSO4*5H2O
См. также
- Халькантит
- Сульфаты
- Медь
- Соединения меди
- Купорос
- Пищевые добавки
- Сульфат меди(I)
Wikimedia Foundation. 2010.
