- Сульфид лития
-
Сульфид лития 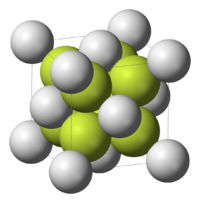
Общие Систематическое наименование Сульфид лития Химическая формула Li2S Эмпирическая формула Li2S Физические свойства Состояние (ст. усл.) твёрдое Молярная масса 46,95 г/моль Плотность 1,66[1] г/см³ Термические свойства Температура плавления 950[1] °C Температура кипения 1527[2] °C Энтальпия образования (ст. усл.) −447[3] кДж/моль Классификация Рег. номер CAS 12136-58-2 Рег. номер EINECS 235-228-1 RTECS OJ6439500 Сульфи́д ли́тия, сернистый литий — Li2S, неорганическое бинарное соединение, литиевая соль сероводородной кислоты.
Содержание
Физические свойства
Сульфид лития представляет собой светло-жёлтое[1] или бесцветное кристаллическое вещество[4], характеризующееся гранецентрированной кубической решёткой типа флюорита[5] (a = 0,571 нм, z = 4, пространственная группа Fm3m[6]), хорошо растворимое в воде, растворимое в спирте. Не образует кристаллогидратов.
Основные термодинамические характеристики[3]:
- стандартная энтальпия образования, ΔHo298 = −447 кДж/моль;
- стандартная энтропия образования, So298 = 63 Дж/(моль·K);
- стандартная энергия Гиббса образования, ΔGo298 = −439 кДж/моль.
Химические свойства
- Пропуская через водный раствор сероводород, реакцию гидролиза можно сместить вправо:
- Образующийся сильно гигроскопичный гидросульфид лития можно выделить в чистом виде[5].
- Водный раствор под действием кислорода воздуха на холоду постепенно окисляется, образуя осадок элементарной серы:
- Во влажном воздухе вещество постепенно окисляется до тиосульфата[4]:
- При действии окислителей (O2, KClO3, PbO2 и пр.) при нагревании свыше 300 °C сульфид лития окисляется до сульфата[1]:
- Вступает в реакции с разбавленными кислотами с выделением сероводорода:
- Являясь сильным восстановителем, с концентрированными серной и азотной кислотами, сульфид лития вступает в окислительно-восстановительные реакции:
Получение
Одна из потенциальных проблем при получении сульфида лития заключается в легкости его окисления, особенно в присутствии воды. Кроме того, вследствие гидролиза препаративные методы, основанные на реакциях обмена в водных растворах, обычно непригодны.
Так как сульфид лития не встречается в природе в виде минерального сырья, существуют следующие промышленные способы его получения[1][7]:
- взаимодействие гидрида лития с элементарной серой при температуре 300-350 °C:
- прокаливание оксида или карбоната лития в токе сухого сероводорода при температуре 900-1000 °C:
- восстановление сульфата лития коксом или водородом при высоких температурах:
Среди прочих возможных методов производства можно отметить[9]:
- взаимодействие гидроксида лития с газообразной серой при температуре до 445 °C:
- взаимодействие гидроксида лития с сероводородом в среде апротонного органического растворителя:
Полисульфиды лития
Для лития, в отличие от других щелочных металлов, полисульфиды не являются характерными соединениями и их получение требует особых условий[10][5].
Наиболее изучены[5]:
 — дисульфид лития, жёлтый порошок, получаемый кипячением спиртового раствора гидросульфида лития с избытком серы в токе водорода:
— дисульфид лития, жёлтый порошок, получаемый кипячением спиртового раствора гидросульфида лития с избытком серы в токе водорода: — тетрасульфид лития, неустойчивое вещество, получаемое реакцией лития с серой в жидком аммиаке:
— тетрасульфид лития, неустойчивое вещество, получаемое реакцией лития с серой в жидком аммиаке:



Применение
Сульфид лития входит в состав анодов[11] и твёрдого электролита для литиевых элементов питания (батареек и аккумуляторов)[12]. Также используется как депиляционный агент в косметических средствах[13].
Может использоваться как компонент в производства стёкол с высокой ионной проводимостью[14].
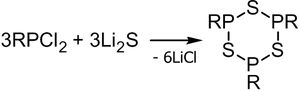
В современной органической химии сульфид лития иногда используется в качестве сульфидирующего агента, например, в следующей реакции[15]:
Также имеются данные об использовании этого вещества в качестве катализатора при защите гидроксильных групп через получение триметилсилилового эфира[16].
Опасность для здоровья
Опасность для здоровья сульфида лития определяется как токсичностью ионов лития из-за хорошей растворимости соединения в воде, так и токсичностью сероводорода, образующегося вследствие гидролиза этой соли.
Литий поражает центральную нервную систему, вызывая тремор рук, тошноту, повышенное мочеиспускание, нечленораздельность речи, вялость, сонливость, головокружение, жажду. Эффекты от длительного воздействия — апатия, анорексия, утомляемость, летаргия, мышечная слабость, изменения в ЭКГ. Долговременное токсическое действие вызывает гипотиреоз, лейкоцитоз, отёк и увеличение веса, полидипсию/полиурию, нарушение памяти, конвульсии, почечную недостаточность, шок, гипотонию, сердечные аритмии, кому, смерть[17].
Сероводород вызывает раздражение слизистых оболочек глаз и дыхательных путей[17].
Примечания
- ↑ 1 2 3 4 5 6 Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ / Под редакцией проф. Р.А.Лидина. — 3-е изд.. — М.: «Химия», 2000. — С. 17. — ISBN 5-7245-1163-0
- ↑ Lithium Sulfide (англ.). The Chemical Database. Hardy Research Group, Department of Chemistry, The University of Akron. Архивировано из первоисточника 7 апреля 2012. Проверено 17 сентября 2009.
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 483. — ISBN 5-7107-8085-5
- ↑ 1 2 Турова Н.Я. Неорганическая химия в таблицах. — М.: Высший химический колледж РАН, 1997. — С. 85.
- ↑ 1 2 3 4 5 6 Плющев В.Е., Степанов Б.Д. Химия и технология соединений лития, рубидия и цезия. — М.: «Химия», 1970. — С. 37-38.
- ↑ 1 2 Литий // Химическая энциклопедия / Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988. — Т. 1. — С. 1201-1202.
- ↑ Sulfides (англ.). Technical Publications. Cerac Inc. Архивировано из первоисточника 4 декабря 2012. Проверено 18 сентября 2009.
- ↑ Данный способ можно рекомендовать также в качестве лабораторного.
- ↑ Method of manufacturing lithium sulfide (англ.). FreePatentsOnline. Архивировано из первоисточника 7 апреля 2012. Проверено 18 сентября 2009.
- ↑ Полисульфиды калия и натрия могут быть получены простым сплавлением твердых компонентов (серы и сульфида металла соответственно). Для сульфида лития этот способ неприменим.
- ↑ Henriksen G., Kaun T., Jansen A., Prakash J., Vissers D. Advanced cell technology for high-perfomance Li-Al/FeS2 secondary batteries // Molton Salts XI / Edited by H. C. De Long, P. C. Trulove, S. Deki, G. R. Stafford. — Proceedings Series. — Pennington, New Jersey, USA: The Electrochemical Society, Inc., 1998. — P. 302-305. — ISBN 1-56677-205-2
- ↑ Tatsumisago M, Wakihara M, Iwakura C, Kohjiya S, Tanaka I. Solid state ionics for batteries / Editor-in-chief: Minami T. — Springer, 2005. — P. 32. — ISBN 978-4-431-24974-0
- ↑ Depilating Ingredients (англ.). MakingCosmetics.com Inc. Архивировано из первоисточника 7 апреля 2012. Проверено 17 сентября 2009.
- ↑ Зарецкая Г.Н. Влияние содержания сульфида лития на свойства и структуру стекол системы LiPO3-Li2S (pdf). Российская Академия Естествознания. Архивировано из первоисточника 7 апреля 2012. Проверено 18 сентября 2009.
- ↑ Devillanova F. A. Handbook of chalcogen chemistry: new perspectives in sulfur, selenium and tellurium. — Royal Society of Chemistry, 2006. — P. 312. — ISBN 978-0-85404-366-8
- ↑ Bioactive natural products // Studies in Natural Products Chemistry / Edited by Professor Atta-ur Rahman. — Elsevier Ltd., 2000. — Т. 24. — P. 85. — ISBN 978-0-44442-971-1
- ↑ 1 2 Lithium Sulfide (англ.). Material Safety Data Sheets. Electronic Space Products International. Архивировано из первоисточника 7 апреля 2012. Проверено 17 сентября 2009.
Соединения литияАзид лития (LiN3) • Алюминат лития (LiAlO2) • Алюмогидрид лития (LiAlH4) • Амид лития (LiNH2) • Ацетат лития (CH3COOLi) • Ацетиленид лития (Li2C2) • Бензиллитий (LiСH2С6H5) • Бензоат лития (C6H5COOLi) • Бромат лития (LiBrO3) • Бромид лития (LiBr) • Гексафторфосфат лития (LiPF6) • Гидрид лития (LiH) • Гидрокарбонат лития (LiHCO3) • Гидроксид лития (LiOH) • Гидроортофосфат лития (Li2HPO4) • Гидросульфат лития (LiHSO4) • Гидросульфид лития (LiHS) • Гидрофторид лития (LiHF2) • Дигидроортофосфат лития (LiH2PO4) • Дисульфит лития (Li2S2O5) • Дихромат лития (Li2Cr2O7) • Имид лития (Li2NH) • Иодат лития (LiIO3) • Иодид лития (LiI) • Карбид лития (Li2С2) • Карбонат лития (Li2CO3) • Метагерманат лития (Li2GeO3) • Метасиликат лития (Li2SiO3) • Метафосфат лития (LiPO3) • Метиллитий (LiСH3) • Нитрат лития (LiNO3) • Нитрид лития (Li3N) • Нитрит лития (LiNO2) • Оксалат лития (Li2C2O4) • Оксид лития (Li2O) • Ортофосфат лития (Li3PO4) • Пербромат лития (LiBrO4) • Пероксид лития (Li2O2) • Пероксомоносульфат лития (Li2SO5) • Персульфат лития (Li2S2O8) • Перхлорат лития (LiClO4) • Силицид лития (Li6Si2) • Сорбат лития (C6H7LiO2) • Сульфат лития (Li2SO4) • Сульфид лития (Li2S) • Сульфит лития (Li2SO3) • Тетрагидридоалюминат лития (Li[AlH4]) • Тетрагидридоборат лития (Li[BH4]) • Тиоцианат лития (LiSCN) • Фениллитий (LiС6H5) • Формиат лития (HCOOLi) • Фталимид лития • Фторид лития (LiF) • Хлорат лития (LiClO3) • Хлорид лития (LiCl) • Хромат лития (Li2CrO4) • Цианат лития (LiOCN) • Цианид лития (LiCN) • Цианоаурат лития (Li[Au(CN)2] • Этиллитий (LiС2H5) •
Растворимость кислот, оснований и солей в водеH+ Li+ K+ Na+ NH4+ Ba2+ Ca2+ Mg2+ Sr2+ Al3+ Cr3+ Fe2+ Fe3+ Ni2+ Co2+ Mn2+ Zn2+ Ag+ Hg2+ Hg22+ Pb2+ Sn2+ Cu+ Cu2+ OH− P P P — P М Н М Н Н Н — Н Н Н Н Н — — Н Н Н Н F− P Н P P Р М Н Н М Р Н Н Н Р Р М Р Р М М Н Р Н Р Cl− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Н Р Н М — Н Р Br− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Н М Н М Р H Р I− P P P P Р Р Р Р Р Р ? Р — Р Р Р Р Н Н Н Н М Н — S2− P P P P — Р М Н Р — — Н — Н Н Н Н Н Н Н Н Н Н Н SO32− P P P P Р М М М Н ? ? М ? Н Н Н М Н Н Н Н ? Н ? SO42− P P P P Р Н М Р Н Р Р Р Р Р Р Р Р М — Н Н Р Р Р NO3− P P P P Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р — Р — Р Р NO2− P P P P Р Р Р Р Р ? ? ? ? Р М ? ? М ? ? ? ? ? ? PO43− P Н P P — Н Н Н Н Н Н Н Н Н Н Н Н Н Н ? Н Н Н Н CO32− М Р P P Р Н Н Н Н — — Н — Н Н — Н Н — Н — — ? — CH3COO− P Р P P Р Р Р Р Р — Р Р — Р Р Р Р Р Р М Р — Р Р CN− P Р P P Р Р Р Р Р ? Н Н — Н Н Н Н Н Р Н Р — — Н SiO32− H Н P P ? Н Н Н Н ? ? Н ? ? ? Н Н ? ? ? Н ? ? ? Категории:- Соединения лития
- Сульфиды
- Бинарные соединения
Wikimedia Foundation. 2010.

![\mathsf{Li_2S+8H_2O=2[Li(H_2O)_4]^++S^{2-}}](243d68b0a086593d91b7c2a52dc35810.png)