- Глибенкламид
-

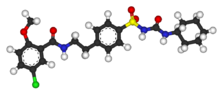 Глибенкламид
ГлибенкламидХимическое соединение ИЮПАК 5-chloro-N-(4-[N-(cyclohexylcarbamoyl)sulfamoyl]phenethyl)-2-methoxybenzamide Брутто-
формулаC23H28ClN3O5S Мол.
масса494,004 г/моль CAS PubChem DrugBank Классификация АТХ Фармакокинетика Связывание с белками плазмы Extensive Метаболизм Гидроксилирование в печени (CYP2C9-mediated) Период полувыведения 10 часов Экскреция Почки и Печень Лекарственные формы Твёрдая (таблетки) Способ введения Внутрь (Per os) Глибенклами́д (син. Антибет, Апоглибурид, Ген-глиб, Гилемал, Глибамид, Глибенкламид Тева, Глибурид, Глюкобене, Даонил, Дианти, Манинил, Эугликон) — представитель второго поколения производных сульфонилмочевины, один из самых популярных и изученных сахароснижающих препаратов, который с 1969 года широко применяется во многих странах мира как надёжное и проверенное средство терапии сахарного диабета 2-го типа при неэффективности мероприятий по изменению образа жизни[1].
Несмотря на появление новых препаратов сульфонилмочевины с улучшенными характеристиками, а также противодиабетических медикаментов с другими механизмами действия, ставить точку в истории глибенкламида рано — в экспериментальных и клинических исследованиях данный препарат не только является эталоном для оценки эффективности новых молекул и терапевтических подходов, но и демонстрирует потенциально полезные дополнительные свойства[2].
Содержание
Механизм действия
Основной механизм действия глибенкламида, как и других представителей препаратов сульфонилмочевины, хорошо изучен на молекулярно-рецепторном уровне. Глибенкламид блокирует АТФ-зависимые калиевые каналы (К+-АТФ-каналы), локализующиеся на плазматической мембране бета-клеток поджелудочной железы.[3] Прекращение поступления в клетку калия приводит к деполяризации мембраны и притоку ионов Ca+ через потенциалзависимые кальциевые каналы. Повышение внутриклеточного содержания кальция посредством активации кальций/кальмодулинзависимой протеинкиназы II стимулирует экзоцитоз секреторных гранул с инсулином, в результате чего гормон проникает в межклеточную жидкость и кровь. Неодинаковая аффинность препаратов сульфонилмочевины к рецепторам бета-клеток обусловливает их различную сахароснижающую активность. Глибенкламид обладает самым высоким сродством к рецепторам сульфонилмочевины на бета-клетках и наиболее выраженным сахароснижающим эффектом среди препаратов сульфонилмочевины[4].
Эффект стимуляции секреции инсулина напрямую зависит от принятой дозы глибенкламида и проявляется как в условиях гипергликемии, так и при нормогликемии или гипогликемии[5][6].
Вся группа препаратов сульфонилмочевины в той или иной степени оказывают периферические (внепанкреатические) эффекты, которые заключаются в повышении чувствительности периферических тканей, в первую очередь жировой и мышечной, к действию инсулина и улучшении усвоения глюкозы клетками[7].
Эффективность и безопасность
Этот раздел статьи ещё не написан. Согласно замыслу одного из участников Википедии, на этом месте должен располагаться специальный раздел.
Вы можете помочь проекту, написав этот раздел.Новые горизонты
Этот раздел статьи ещё не написан. Согласно замыслу одного из участников Википедии, на этом месте должен располагаться специальный раздел.
Вы можете помочь проекту, написав этот раздел.Премия Кройцфельда-2010
Премия Кройцфельда — ежегодная премия за достижения в области фармакологии. Названа в честь немецкого нейропатогистолога Ганса Герхарда Кройцфельда (1885—1964).
Значение глибенкламида, в частности его микронизированной формы, для мировой диабетологии было по достоинству оценено престижной фармацевтической премией Крейцфельда (H. G. Creutzfeldt Drug Prize) - Выбор Практикующих врачей, присуждённой в июле 2010 года за разработку препарата Манинил в рамках ежегодного конкурса лекарственных средств, который проводится Институтом имени Г. Г. Кройцфельда (г. Киль, Германия)[2].
Этот раздел статьи ещё не написан. Согласно замыслу одного из участников Википедии, на этом месте должен располагаться специальный раздел.
Вы можете помочь проекту, написав этот раздел.См. также
Примечания
- ↑ Клиническая эндокринология. Руководство / Старкова Н. Т. — 3-е изд., перераб. и доп. — СПб.: Питер, 2002. — С. 259—262. — 576 с. — («Спутник Врача»). — 4000 экз. — ISBN 5-272-00314-4
- ↑ 1 2 Панькив В.И. Глибенкламид в XXI веке: хорошо не забытое старое // International jornal of endocrinology. — 2010. № 7 (31). С. 63—70.
- ↑ Serrano-Martín X, Payares G, Mendoza-León A (December 2006). «Glibenclamide, a blocker of K+(ATP) channels, shows antileishmanial activity in experimental murine cutaneous leishmaniasis». Antimicrob. Agents Chemother. 50 (12): 4214–6. DOI:10.1128/AAC.00617-06. PMID 17015627.
- ↑ Lebovitz H. E. Insulin secretagogues: old and new // Diabetes Rev. — 1999. — Vol. 7, № 3. — P. 139—153.
- ↑ Groop L., Barzilai N., Ratheiser K. et al. Dose-dependent effects of glyburide on insulin secretion and glucose uptake in humans // Diabetes Care. — 1991. — Vol. 14. — P. 724—727/
- ↑ Groop L., Luzi L., Melanger A. et al. Different effects of glyburide and glipizide on insulin secretion and hepatic glucose production in normal and NIDDM subjects // Diabetes. — 1987. — Vol. 36. — P. 1320—1328.
- ↑ Балаболкин М.И., Креминская В.М., Клебанова Е.М. Современная тактика лечения сахарного диабета типа 2 // Consilium Medicum. — 2001. — T. 3, № 11.
Ссылки
Шаблон:АТХ код A10
Категории:- Лекарственные средства по алфавиту
- Диабетология
- Сахарный диабет
Wikimedia Foundation. 2010.
