- Тиомочевина
-
Тиомочевина 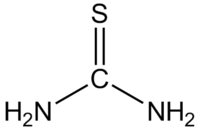
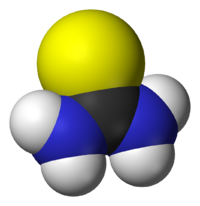
Общие Химическая формула CH4N2S Физические свойства Молярная масса 76,12 г/моль Термические свойства Температура плавления 182 °C Классификация Рег. номер CAS 62-56-6 SMILES C(=S)(N)N Тиомочевина — CS(NH2)2 — диамид тиоугольной кислоты, тиокарбамид, белые кристаллы горького вкуса, tпл 180—182 °C (при быстром нагревании; при медленном — разлагается); умеренно растворима в воде, метаноле, пиридине, хорошо — в 50 %-ном водном пиридине.
Тиомочевину применяют в органическом синтезе, для получения лекарственных препаратов (напр., сульфидина).
Содержание
Синтез
Тиомочевина может быть получена изомеризацией роданида аммония, этот синтез аналогичен классическому синтезу мочевины из цианата аммония (кислородного аналога роданида) по Вёлеру:
Вместе с тем, в отличие от мочевины, тиомочевина при нагревании находится в равновесии с роданидом аммония: равновесная смесь при температуре 140 °C содержит 28,1 % тиомочевины, при 156 °C — 26,7 %, при 180 °C — 21,8 %[1].
Подобно синтезу мочевины из аммиака и диоксида углерода, тиомочевина также быть синтезирована при взаимодействии аммиака и сероуглерода:
Тиомочевину также получают взаимодействием H2S или сульфидов аммония либо щелочных металлов с цианамидом кальция CaCN2 в водных растворах:
Реакционная способность
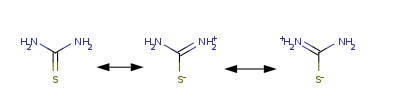
Структура молекулы тиомочевины может быть представлена мезомерными канонической тиоамидной формой и тиоимидными формами, несущими отрицательный заряд на атоме серы и положительный на атомах азота амидинового фрагмента:
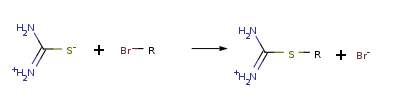
В результате атом серы является сильным нуклеофильным центром и тиомочевина протонируется по атому серы с образованием солей с сильными кислотами. Атаки мягких электрофилов также направляются на атом серы: тиомочевина алкилируется алкилгалогенидами и алкилсульфатами с образованием изотиурониевых солей:
Аналогично протекает реакция тиомочевины с арилдиазониевыми солями.
S-алкилирование тиомочевины также является первой стадией её взаимодействия с эпоксидами, ведущего к образованию тииранов (эписульфидов)[2]:
Ацилирование тиомочевины галогенангидридами и ангидридами карбоновых кислот, в зависимости от условий реакции, может протекать как сере (в мягких условиях), так и по азоту (в жестких условиях).
Альдегиды и кетоны с присоединяются к тиомочевине, образуя гидроксиалкилтиомочевины, которые при отщеплении воды превращаются в N-тиокарбамоилимины:
- H2NC(S)NH2 + R2CO
 H2NC(S)NHC(OH)R2
H2NC(S)NHC(OH)R2 - H2NC(S)NHC(OH)R2
 H2NC(S)N=CR2
H2NC(S)N=CR2
Тиомочевина реагирует с бифункциональными электрофилами, образуя гетероциклические соединения. Так, например, с α-галогенкетонами тиомочевина (и её N-замещенные производные)образует 2-аминотиазолы:
при взаимодействии с 1,3-дикарбонильными соединениями - 2-меркаптопиримидины:
Применение
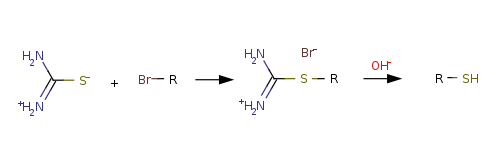
Алкилирование тиомочевины используется алкилирование с образованием алкилтиурониевых солей и их последующим щелочным гидролизом: используется как препаративный метод синтеза алифатических тиолов:
Преимуществом этого метода являются легкая очистка перекристаллизацией тиурониевых солей и достаточно высокие общие выходы тиолов.
Тиомочевина также широко используется в синтезе гетероциклических соединений, а также в качестве ингибитора кислотной коррозии сталей.
Примечания
- ↑ Тиомочевина // Большая Химическая Энциклопедия
- ↑ Zeynizadeh, Behzad; Samal Yeghaneh (2008). «Solvent-Free Conversion of Epoxides to Thiiranes by Thiourea/NH4Cl System». Phosphorus, Sulfur, and Silicon and the Related Elements 183 (9): 2280-2286. DOI:10.1080/10426500801960703.
Литература
- О. Я. Нейланд Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1
 Категории:
Категории:- Фитогормоны
- Тиокарбонильные соединения
- Ингибиторы коррозии
-
Wikimedia Foundation. 2010.