- Дигидроксиацетон
-
Дигидроксиацетон 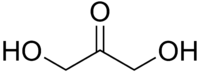

Общие Систематическое наименование 1,3-дигидроксипропанон-2 Традиционные названия Дигидроксиацетон, глицерон Химическая формула СН2(ОН)-СО-СН2(ОН) Эмпирическая формула C3H6O3 Физические свойства Отн. молек. масса 90,078 а. е. м. Молярная масса 90,078 г/моль Плотность 1,372 г/см³ Термические свойства Температура плавления 90 °C Классификация Рег. номер CAS 96-26-4 SMILES O=C(CO)CO Дигидроксиацетон (глицерон, 1,3-дигидроксипропанон-2) — моносахарид из группы триоз с эмпирической формулой C3H6O3. Является простейшим представителем кетосахаров (кетоз) и единственным представителем группы кетотриоз.[1][2]
Содержание
Строение молекулы
Дигидроксиацетон, будучи самым простым из всех кетоз, не имеет асимметричного атома углерода (хирального центра) и, как следствие, не обладает оптической активностью. В кристаллическом состоянии и в свежеприготовленном водном растворе дигидроксиацетон существует в виде циклический димера. Спустя некоторое время в растворе димер распадается.[2]
Структурным изомером дигидроксиацетона является глицеральдегид.
Физические и химические свойства
Дигидроксиацетон представляет собой гигроскопичное белое кристаллическое вещество, обладающее сладким вкусом и характерным запахом. В хорошо растворим в воде, гораздо хуже растворим в этиловом спирте, диэтиловом эфире, ацетоне, толуоле и других неполярных растворителях.[3]
Дигидроксиацетон вступает практически во все реакции типичные для кетонов, например с фенилгидразином он дает гидразон и затем озазон (тождественный озазону глицеральдегида). Присоединяет синильную кислоту, образуя гидроксинитрилы. В то же время, из-за того, что гидроксильные группы находится при атоме углерода, соседнем с карбонильной группой, дигидроксиацетон является сильным восстановителем и вступает в реакции более свойственные альдегидам. Так он заимодействует с фуксинсернистой кислотой, восстанавливает аммиачный раствор оксида серебра(I) и фелинговой жидкости (при этом происходит расщепление его молекулы).
Активными восстановителями (боргидриды или алюмогидриды щелочных металлов) дигидроксиацетон восстанавливается до глицерина.
Биологическая роль, получение и применение
Дигидроксиацетон в фосфорилированной форме (дигидроксиацетонфосфат) принимает участие в гликолизе, являясь промежуточным продуктом метаболизма фруктозы. В биохимических реакциях под действием фермента триозофосфатизомеразы дигидроксиацетон вступает во взаимопревращения с глицеральдегидом.[4]
Дигидроксиацетон, связывая SO2, влияет на микробную активность в вине, что делает его присутствие в винах нежелательным.[5]
Способность дигидроксиацетона окрашивать кожу в темный цвет предопределила его использование в качестве широко распространенного ингредиента в средствах для загара.[6]
Для косметических целей дигидроксиацетон получают из растительных источников (в основном из сахарной свеклы и сахарного тростника) или из глицерина, путем ферментативного окисления при помощи сорбозных бактерий.[6]
Для целей препаративной химии дигидроксиацетон синтезируют химическим путем — мягким окислением глицерина пероксидом водорода в присутствии катализатора (диоксида марганца). Также используется более современный метод окисления глицерина кислородом воздуха на в присутствии палладия и неокупроина в качестве катализаторов.[7]
Примечания
- ↑ Thisbe K. Lindhorst Essentials of Carbohydrate Chemistry and Biochemistry. — 1st. — Wiley-VCH, 2007. — ISBN 3-527-31528-4
- ↑ 1 2 Чичибабин, А. Е. Основные начала органической химии: Т. 2 / А. Е. Чичибабин. — 6 изд.. — М.:Наука, 1958. — 974 с.
- ↑ Рабинович, В. А. Краткий химический справочник / В. А. Рабинович, З. Я. Хавин. – 2-е изд. испр. и доп. – Л.: Химия, 1978. – 392 с.
- ↑ Племенков, В. В. Введение в химию природных соединений /В. В. Племенков. – Казань, 2001. – 376 с.
- ↑ Eschenbruch R, Dittrich HH. (1986). «Metabolism of acetic acid bacteria in relation to their importance to wine quality». Zentrablatt für Mikrobiologie 141: 279–289.
- ↑ 1 2 Самуйлова, Л. И. Косметическая химия в 2 ч.: Часть 1: Ингредиенты / Л. И. Самуйлова, Т. А. Пучкова. - М.: Школа косметических химиков, 2005. - 386 с
- ↑ Painter, R. M., Pearson, D. M. and Waymouth, R. M. (2010), Selective Catalytic Oxidation of Glycerol to Dihydroxyacetone. Angewandte Chemie International Edition, 49: 9456–9459. doi: 10.1002/anie.201004063.
Литература
- Каррер, П. Курс органической химии. - М.: Химия, 1960. - 1216 с.
- Кочетков, Н.К. Химия углеводов / Н. К. Кочетков, А. Ф. Бочков, Б. А. Дмитриев. – М.: Наука, 1967. – 672 с.
- Березин, Б. Д. Курс современной органической химии: Учебное пособие / Б. Д. Березин. – М: Высшая школа, 1999. – 768 с.
- Чичибабин, А. Е. Основные начала органической химии: Т. 2 / А. Е. Чичибабин. — 6 изд.. — М.:Наука, 1958. — 974 с.
См. также

Углеводы Общие: Альдозы · Кетозы · Фуранозы · Пиранозы Геометрия Аномеры · Мутаротация · Проекция Хоуорса Моносахариды Диозы Альдодиоза (Гликольальдегид) Триозы Кетотриоза (Дигидроксиацетон) · Альдотриоза (Глицеральдегид) Тетрозы Кетотетроза (Эритрулоза) · Альтотетрозы (Эритроза, Треоза) Пентозы Кетопентозы (Рибулоза, Ксилулоза) Альдопентозы (Рибоза, Арабиноза, Ксилоза, Ликсоза)
Дезоксисахариды (Дезоксирибоза)Гексоза Кетогексозы (Псикоза, Фруктоза, Сорбоза, Тагатоза) Альдогексозы (Аллоза, Альтроза, Глюкоза, Манноза, Гулоза, Идоза, Галактоза, Талоза)
Дезоксисахариды (Фукоза, Фукулоза, Рамноза)Гептозы Кетогептозы (Седогептулоза, Манногептулоза) >7 Октозы · Нанозы (Нейраминовая кислота) Мультисахариды Дисахариды Сахароза · Лактоза · Мальтоза · Трегалоза · Тураноза · Целлобиоза · Мелибиоза · Генцибиоза · Вицианоза · Апиоза · Рутиноза Трисахариды Рафиноза · Мелицитоза · Мальтотриоза · Генцианоза · Солатриоза · Целлотриоза Тетрасахариды Акарбоза · Стахиоза Олигосахариды Фруктан · Галактан · Маннан · Изомальтан · Ксилан · Арабан Полисахариды Гликоген · Крахмал · Целлюлоза · Хитин · Амилоза · Амилопектин · Сахилоза · Инулин · Декстран · Пектин · Галактоманнан · Агароза · Лихенин · Пуллулан Производные углеводов Аминосахара · Фосфосахара · Ангидросахара · Гликозиды · N-Гликозиды · Гликали · Гликоны · Енозы · Гликозеены · Гликозаны · Гликаны · Глюканы Гликозаминогликаны Гепарин · Гепаринсульфат · Хондроитин · Хондроитинсульфат · Гиалуроновая кислота · Гепаран · Дерматан · Дермантансульфат · Кератан · Кератансульфат · Пептидогликан · Хитозамин · Хондрозамин Аминогликозиды Канамицин · Стрептомицин · Тобрамицин · Неомицин · Паромомицин · Апрамицин · Гентамицин · Нетилмицин · Амикацин Категории:- Триозы
- Кетозы
- Косметические вещества
Wikimedia Foundation. 2010.

